Первый закон термодинамики
Рассмотрим любой термодинамический цикл. Несмотря на то, что баланс входящей и выходящей энергии соблюдается – иначе процесс был бы незамкнут и цикла не получилось бы – баланса входящей и выходящей работы и энергии нет. Соответственно основная задача любого термодинамического ( в дальнейшем Т°-дин.) цикла – преобразование теплоты в работу или работы в теплоту. Прямой цикл преобразует теплоту в работу, обратный ( или холодильный) – работу в теплоту.
<br/>Первый закон Т°-дин. как аксиому предполагает что в замкнутых Т°-дин. системах соблюдается баланс внутренней и подведенной внешней энергий и отведенной теплотой. На практике он формулируется как dU = dQ – dL , т.е. изменение внутренней энергии системы равно количеству теплоты, отведенному от системы, за вычетом работы, над системой совершён...
реклама
Рассмотрим любой термодинамический цикл. Несмотря на то, что баланс входящей и выходящей энергии соблюдается – иначе процесс был бы незамкнут и цикла не получилось бы – баланса входящей и выходящей работы и энергии нет. Соответственно основная задача любого термодинамического ( в дальнейшем Т°-дин.) цикла – преобразование теплоты в работу или работы в теплоту. Прямой цикл преобразует теплоту в работу, обратный ( или холодильный) – работу в теплоту.
Первый закон Т°-дин. как аксиому предполагает что в замкнутых Т°-дин. системах соблюдается баланс внутренней и подведенной внешней энергий и отведенной теплотой. На практике он формулируется как dU = dQ – dL , т.е. изменение внутренней энергии системы равно количеству теплоты, отведенному от системы, за вычетом работы, над системой совершённой.
Причем, что важно, правило это соблюдается не только глобально, но и локально. Рассматривая любой отрезок цикла мы можем, точно зная два параметра, определить третий.
Здесь мы подходим к очень важному, если не важнейшему, параметру любого Т°-дин. цикла – энтальпии.
Как и любая другая функция состояния, в любой выбранной точке цикла эта функция неизменна и выражает собой ( грубо говоря )внутреннюю удельную или абсолютную энергию системы относительно некоторой начальной точки. В различных таблицах эта величина отсчитывается и от 0°С и 1 атм. и от 20°С и от чего-либо ещё. Это не важно, потому что, как и в случае с напряжением, имеет смысл лишь разность энтальпий ( изменение внутренней энергии системы) на каком-либо участке Т°-дин. цикла.
Определения первого закона термодинамики:
Теплота, подведенная к Т°-дин. системе, расходуется на совершение работы и изменение внутренней энергии системы.
Для изолированных систем внутренняя энергия постоянна.
Вопрос на засыпку – может ли сжатый газ совершать работу сам по себе? Не приводя в действие турбину, а совершенно самодостаточно? Если действие происходит в вакууме – то однозначно «нет», но в реальной жизни существует такое понятие « выхлоп». Выброс малого количества сжатого газа в большой объем газа, относительного разреженного. Представьте себе ( а лучше купите и попробуйте сами) надутие воздушного шарика или, что интереснее, сверхтонкого презерватива. Растянуть презерватив – не так уж и сложно, но при надутии требуется постоянно подводить к нашей Т°-дин. системе работу легких, с натугой выдувающих воздух, которая много больше работы по растягиванию. Так на что же уходит работа? На расталкивание молекул воздуха вне оболочки нашего воздушного шарика! Причем, как можно легко понять, представив этот процесс, количество требуемой энергии прямо пропорционально объему, который требуется вытолкнуть и внешнему давлению.
Формулируем : dL = p* dV
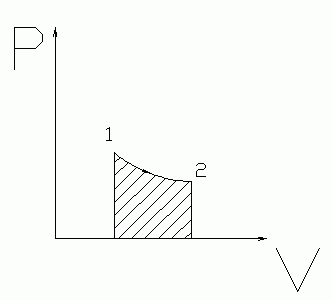
Для равновесных процессов суммарная работа будет равна сумме изменения объема помноженного на давление для каждого равновесного состояния. А, так как, равновесных состояний бесконечное количество,работа процесса в P-V диаграмме будет численно равна площади под графиком процесса. И, если объем увеличивается, работа газом совершается, а если уменьшается – над газом работу совершают.

Ещё раз каснемся энтальпии. Так как в Т°-дин. процессе может совершаться работа самого газа, энтальпию нельзя рассматривать как простой показатель внутренней энергии системы. Рассмотрим чему равно изменение энтальпии:
dh = du + p*dv + v* dp
Всё, кроме v*dp, уже известно. Этот же компонент характеризует техническую работу, совершаемую системой. Предположим, в потоке, разогреваемом теплотой извне, установлена турбинка, отбирающая некоторое количество энергии и, соответственно,вызывающая снижение внутренней энергии системы. Вот эта отбираемая энергия и называется технической работой. Если смотреть на P-V диаграмму, то численно эта работа будет равна площади левее процесса. При снижении давления – техническая работа от системы отводится. При повышении – подводится.

Как видно – энтальпия отражает не только суммарное внешнее воздействие над системой, но и внутренние процессы, происходящие в системе. Избавившись от дифференциала получаем простую формулу:
h = u + p*v
Первый закон Т°-дин. как аксиому предполагает что в замкнутых Т°-дин. системах соблюдается баланс внутренней и подведенной внешней энергий и отведенной теплотой. На практике он формулируется как dU = dQ – dL , т.е. изменение внутренней энергии системы равно количеству теплоты, отведенному от системы, за вычетом работы, над системой совершённой.
Причем, что важно, правило это соблюдается не только глобально, но и локально. Рассматривая любой отрезок цикла мы можем, точно зная два параметра, определить третий.
Здесь мы подходим к очень важному, если не важнейшему, параметру любого Т°-дин. цикла – энтальпии.
Как и любая другая функция состояния, в любой выбранной точке цикла эта функция неизменна и выражает собой ( грубо говоря )внутреннюю удельную или абсолютную энергию системы относительно некоторой начальной точки. В различных таблицах эта величина отсчитывается и от 0°С и 1 атм. и от 20°С и от чего-либо ещё. Это не важно, потому что, как и в случае с напряжением, имеет смысл лишь разность энтальпий ( изменение внутренней энергии системы) на каком-либо участке Т°-дин. цикла.
Определения первого закона термодинамики:
Теплота, подведенная к Т°-дин. системе, расходуется на совершение работы и изменение внутренней энергии системы.
Для изолированных систем внутренняя энергия постоянна.
Вопрос на засыпку – может ли сжатый газ совершать работу сам по себе? Не приводя в действие турбину, а совершенно самодостаточно? Если действие происходит в вакууме – то однозначно «нет», но в реальной жизни существует такое понятие « выхлоп». Выброс малого количества сжатого газа в большой объем газа, относительного разреженного. Представьте себе ( а лучше купите и попробуйте сами) надутие воздушного шарика или, что интереснее, сверхтонкого презерватива. Растянуть презерватив – не так уж и сложно, но при надутии требуется постоянно подводить к нашей Т°-дин. системе работу легких, с натугой выдувающих воздух, которая много больше работы по растягиванию. Так на что же уходит работа? На расталкивание молекул воздуха вне оболочки нашего воздушного шарика! Причем, как можно легко понять, представив этот процесс, количество требуемой энергии прямо пропорционально объему, который требуется вытолкнуть и внешнему давлению.
Формулируем : dL = p* dV
Для равновесных процессов суммарная работа будет равна сумме изменения объема помноженного на давление для каждого равновесного состояния. А, так как, равновесных состояний бесконечное количество,работа процесса в P-V диаграмме будет численно равна площади под графиком процесса. И, если объем увеличивается, работа газом совершается, а если уменьшается – над газом работу совершают.
Ещё раз каснемся энтальпии. Так как в Т°-дин. процессе может совершаться работа самого газа, энтальпию нельзя рассматривать как простой показатель внутренней энергии системы. Рассмотрим чему равно изменение энтальпии:
dh = du + p*dv + v* dp
Всё, кроме v*dp, уже известно. Этот же компонент характеризует техническую работу, совершаемую системой. Предположим, в потоке, разогреваемом теплотой извне, установлена турбинка, отбирающая некоторое количество энергии и, соответственно,вызывающая снижение внутренней энергии системы. Вот эта отбираемая энергия и называется технической работой. Если смотреть на P-V диаграмму, то численно эта работа будет равна площади левее процесса. При снижении давления – техническая работа от системы отводится. При повышении – подводится.
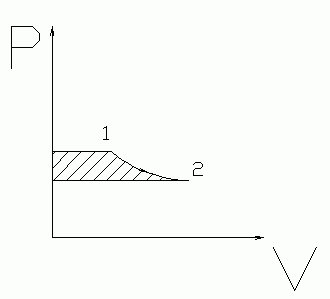
Как видно – энтальпия отражает не только суммарное внешнее воздействие над системой, но и внутренние процессы, происходящие в системе. Избавившись от дифференциала получаем простую формулу:
h = u + p*v
Лента материалов
Правила размещения комментариев
Соблюдение Правил конференции строго обязательно!
Флуд, флейм и оффтоп преследуются по всей строгости закона!
Комментарии, содержащие оскорбления, нецензурные выражения (в т.ч. замаскированный мат), экстремистские высказывания, рекламу и спам, удаляются независимо от содержимого, а к их авторам могут применяться меры вплоть до запрета написания комментариев и, в случае написания комментария через социальные сети, жалобы в администрацию данной сети.


